产品名称:五种致泻性大肠埃希氏菌核酸多重检测试剂盒(PCR-荧光探针法)
英文名称:Multiplex PCR Detection Kit for Diarrheogenic Escherichia coli(Fluorescent Probe Assays)
产品编号与包装规格:
| 编号 | 规格 |
|---|---|
| FZ022BF2 | 48 测试/盒 |
产品简介:本试剂盒仅适用于食品中产志贺毒素(STEC)/肠道出血性(EHEC)、肠道致病性(EPEC)、肠道集聚性(EAEC)、肠道侵袭性(EIEC)、产肠毒素(ETEC)大肠埃希氏菌的毒力基因和类型判别的定性检测。
检测原理:基于Real Time PCR技术,利用针对《GB4789.6-2016》中的12个毒力基因设计的引物、荧光探针以及其他反应优化配置所需试剂组合成A、B、C三管体系,同时往三管体系加入待检样品即可进行扩增反应。在发生扩增过程中,荧光探针与目的基因片段结合,可被Taq酶分解并产生荧光信号,此时荧光定量PCR仪可识别该荧光信号,同时根据其强弱变化绘制出相应的实时扩增曲线,进而判定大肠埃希氏菌的致泻类型。
A管体系可用于STEC/EHEC、EPEC检测,B管体系可用于EAEC检测和大肠埃希氏菌种属鉴定,C管体系可用于ETEC、EIEC检测。
五种致泻性大肠埃希氏菌核酸多重检测试剂盒(PCR-荧光探针法)产品组分:
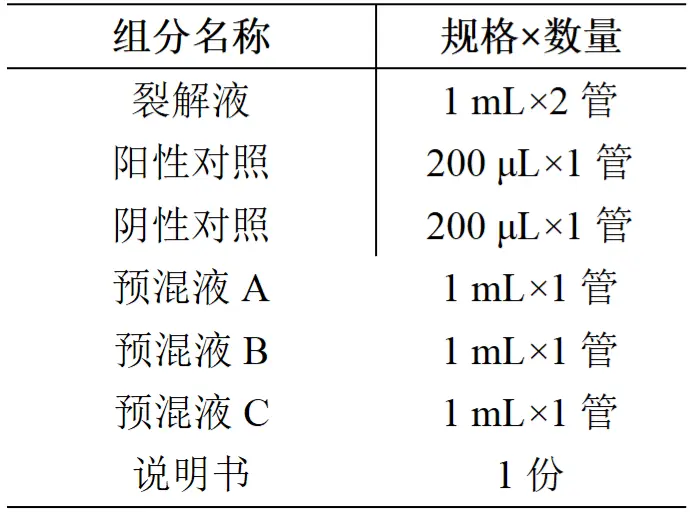
储存条件与保质期:-20℃避光储存,有效期为12个月,避免反复冻融。冷冻条件下运输。
灵敏度:单通道最低检验限达到100~500 cfu/Test。
所需其他材料和适用仪器:荧光定量PCR仪(具有能够检测FAM、VIC、Cy5、ROX标记的荧光通道)、高速离心机、移液器、移液枪头及离心管等。
五种致泻性大肠埃希氏菌核酸多重检测试剂盒(PCR-荧光探针法)使用指南:
1,样品前处理:参照 GB 4789.6−2016,使用 1 μL 接种环刮取营养琼脂平板或斜面上培养 18 h~24 h 的待鉴定的可疑菌落,悬浮到含 30 μL 裂解液或者无菌水的0.2 mL无菌离心管中,充分悬浮菌体,轻弹管壁消除气泡,99℃加热 10 min; 12000 r/min 离心 15 min,上清即为粗提的DNA,可转移至 0.2 mL 无菌离心管中,在-20℃下可长期保存。也可以选择商业化的细菌基因组提取试剂盒进行提取。
2, 加样、反应
1) 按照需求取n个PCR反应管(n=1管阴性对照+待检测样品数+1管阳性对照),从试剂盒中取出预混液,充分融化,涡旋后短暂离心,以上每管加入20 μL预混液,待用。
2) 向上述n个反应管中分别加入阴性对照、待测样品DNA、阳性对照各5 μL,总反应体积为25 μL。盖紧管盖,短暂离心,立即进行PCR扩增反应。
3) PCR反应体系为25 μL,取FAM、VIC、Cy5、ROX检测通道,在反应阶段2中59℃时收集荧光信号,具体程序如下:
| 反应阶段 | 温度 | 时间 | 信号收集 | 循环数 |
| 1 | 95°C | 1 min | 1 | |
| 2 | 95°C | 20 sec | } 40 | |
| 59°C | 30 sec | ✔ |
3, 结果:一般情况下,可通过软件自动设定的基线、阈值等直接读取检测结果。如需调整,可根据所使用仪器的自身情况(如噪声等)以及选取的不同荧光通道进行调整。
1) 质量控制:阴性对照未出现明显的S型扩增曲线或Ct值>37,阳性对照出现S型扩增曲线且其Ct值<25。若阴阳性对照不同时满足上述条件,则本次检测结果无效,应重新检测或与产品技术支持联系。
2) 结果判读:(根据反应所得Ct值判读,具体见下表:)
| Ct值 | 每个基因判读结果 |
| ≤30 | 对应的基因阳性。 |
| 30~37 | 建议重新检测,若复测结果 Ct≥37,则对应的基因阴性;若重做结果 Ct<37,扩增曲线有明显起峰,该样本判断为阳性。 |
| ≥37 | 对应的基因阴性。 |
各致病型阳性判别标准:
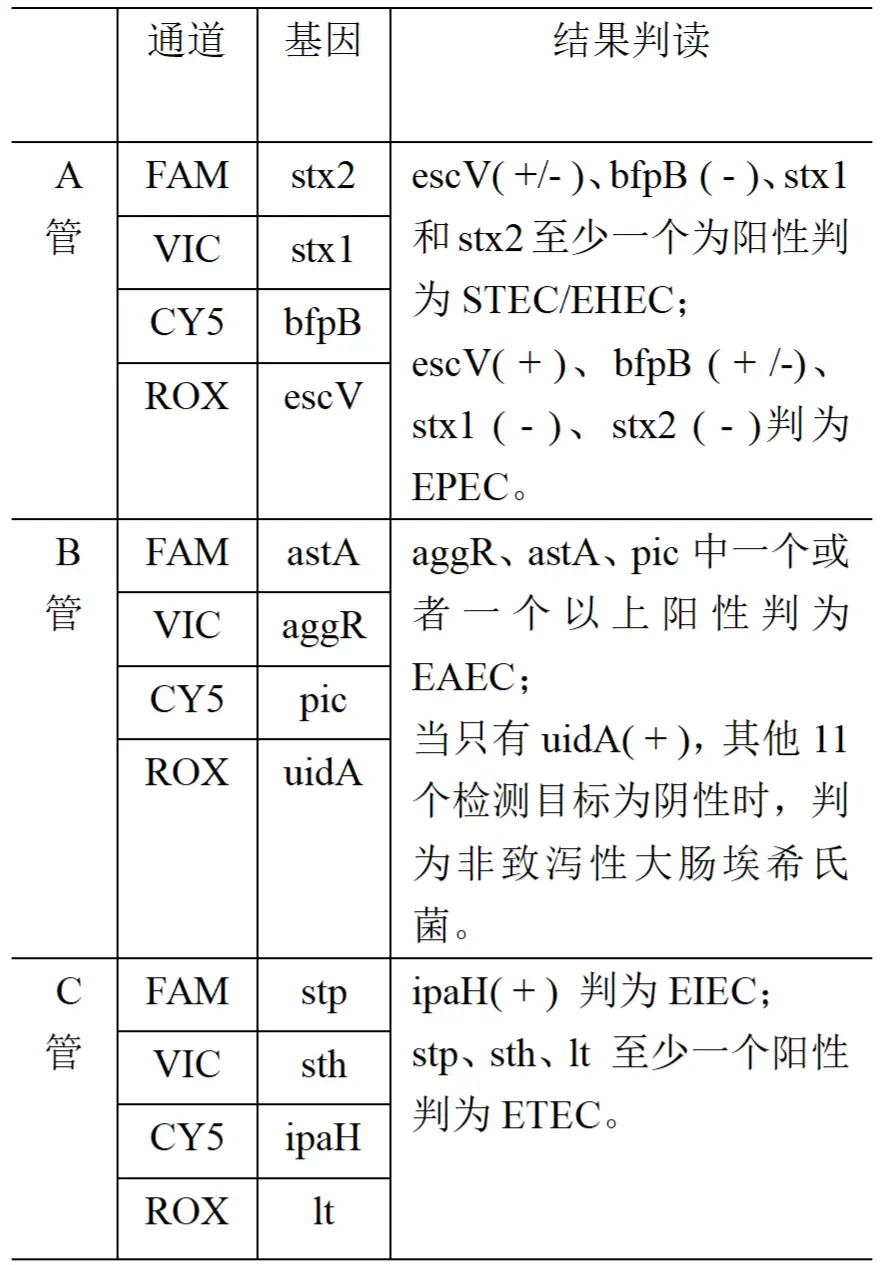
❖ astA和pic基因可在细菌间转移,当与其他DEC毒力基因检测结果同时阳性时,则astA和pic基因不作为型别判定依据。
❖ stp基因灵敏度稍低,为保证检测结果,检测样品的DNA浓度高一点为好。
❖ 一般猪源的ST基因和人源的ST基因在分离的菌株中只存在其中一种,特殊情况下除外。
❖ 多重qPCR检测可能出现不同荧光通道之间竞争抑制的问题,单基因分析时适当调整阈值线。
❖ 部分志贺氏菌会检出ipaH和uidA基因。