光驱动全细胞生物传感器:为硝酸盐检测带来革命性变革
发布时间:2025-02-05 浏览次数:1589
微生物燃料电池(MFC)传感器是一种自再生、通用性强的平台,可开发低成本、易用的分析设备,替代繁琐且昂贵的传统技术。MFC传感器利用电活性细菌(EAB)通过细菌与电极之间的细胞外电子转移EET将分析物转化为电信号,多以阳极模式运行,并通过干扰EAB代谢实现检测,但受限于代谢响应速度和底物依赖性,难以应用于低有机物环境。而反向EET可使细菌从阴极获取电子进行还原反应,效率高且与代谢无关。基于此有研究将悬浮EAB细胞作为传感元件,构建了全细胞生物阴极传感器,灵敏度高并简化了制备过程。当目标分析物可被特定酶感知时,该传感器还具有高选择性。但反向EET驱动的生物阴极反应通常在较低电极电位下进行(低于-0.56 V,相对于SCE),直接用MFC阳极驱动在热力学上不利,而采用三电极系统则与自供能特性相冲突。
将光电极与MFC集成已被验证可以显著提高MFC的性能,光阳极有望驱动生物阴极传感器,但与酶传感器相比,全细胞生物阴极传感器的电子传输路径更为复杂,可能涉及一系列具有不同氧化还原电位的电子传输蛋白。并且由于生物阴极在相对较低的电极电位下运行,必须避免诸如氧气还原和氢气生成等副反应。因此,制备一个具有适当光电化学特性的光阳极以匹配生物阴极的动力学至关重要,这为开发自供能、高效的全细胞生物阴极传感器奠定了基础。在本研究中,顾峥等人首次开发了一种用于硝酸盐检测的自驱动全细胞生物阴极传感器。
1、研究思路与方法:
A. 生物阴极的构建
使用缺乏表达亚硝酸盐还原酶NrfA能力的希瓦氏菌(Shewanella oneidensis MR-1)作为生物催化剂,并补充乳酸钠作为电子供体加速硝酸盐的消耗并显著缩短检测时间。还通过添加1-羟基苯并菲(1-OH phenazine)、中性红(NR)、核黄素(RF)等物质作为可溶性电子穿梭体,优化生物阴极的性能。
B. In₂O₃/In₂S₃光阳极的制备与表征
商业FTO电极乙醇和去离子水清洗后放入聚四氟乙烯衬里的不锈钢高压釜中,加入前驱液(含In(NO₃)₃和NaNO₃),经加热、冲洗、干燥和煅烧后得到In₂O₃修饰的FTO电极(In₂O₃@FTO)。随后使用L-半胱氨酸作为硫源对In₂O₃@FTO进行硫化处理,制备In₂O₃/In₂S₃光阳极。最后使用场发射扫描电子显微镜、X射线衍射和X射线光电子能谱、紫外-可见漫反射光谱(UV–vis DRS)以及线性扫描伏安法(LSV)观察所制备光阳极的形貌、晶体结构和组成、光吸收能力、光电化学特性。
C. 生物阴极传感器的组装与测试
将光阳极与生物阴极通过短路连接,构建了一个自供能的生物传感器。阳极液为0.1 M Na₂SO₃,阴极液为含有M9培养基、18 mM乳酸钠和2 µM 1-羟基苯并菲的细菌悬浮液。通过光照驱动光阳极产生电流,进而为生物阴极提供电子,实现对硝酸盐的还原检测。实验中通过向生物阴极室中添加不同浓度的硝酸盐溶液,记录电流响应,评估传感器的性能。
2、研究结果:
A. 生物阴极对硝酸盐还原的动力学特性:
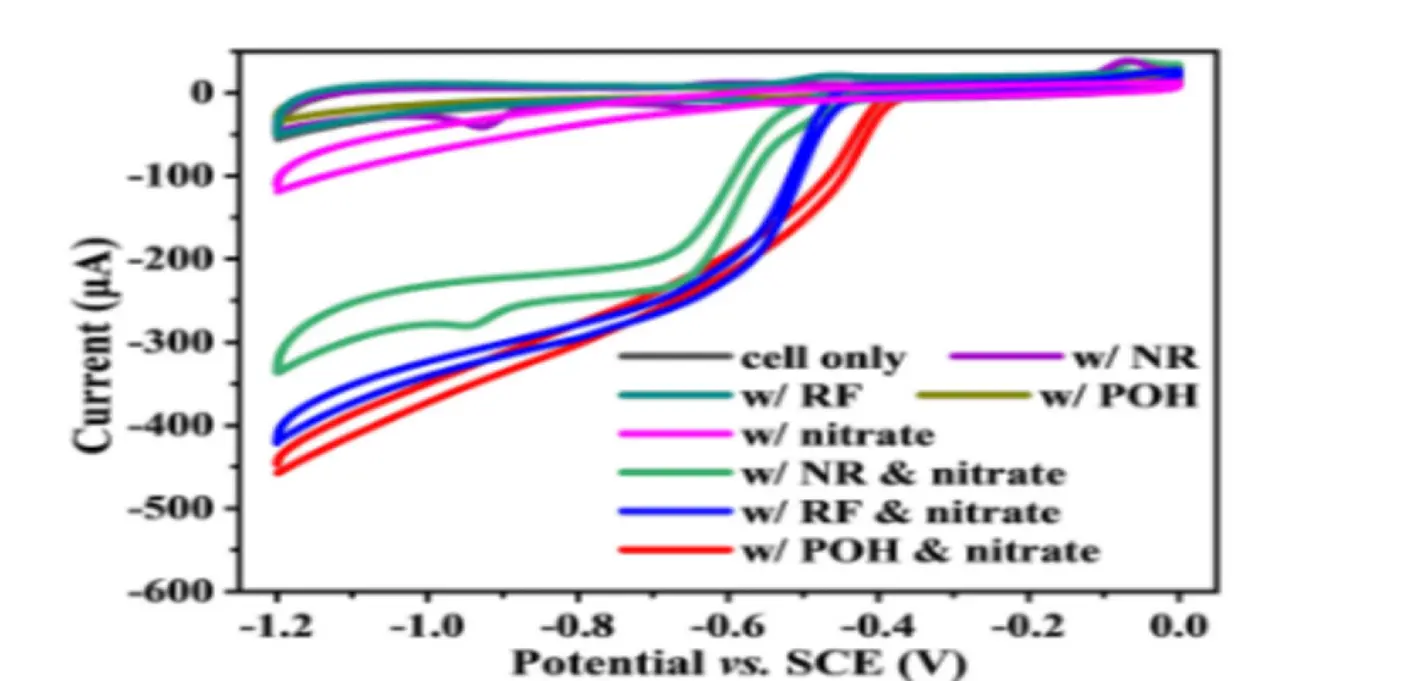
图 1 希瓦氏菌(Shewanella oneidensis MR-1)细胞对硝酸盐还原的循环伏安特性曲线
本研究构建了一个由碳布电极和细菌悬浮液组成的生物阴极,并在10 mM硝酸盐存在下进行循环伏安(CV)分析,以促进细胞外电子传递(EET)。如图1所示,仅在细菌细胞存在时无法区分明显的氧化还原峰,但当加入硝酸盐后,出现了还原电流,表明即使悬浮的细菌细胞也能进行硝酸盐还原的反向电子传递。加入可溶性电子穿梭体后,观察到可逆的氧化还原峰,其表观标准氧化还原电位分别为-0.613 V(中性红,NR)、-0.492 V(核黄素,RF)和-0.472 V(1-羟基苯并菲,POH)。如预期所示,当向生物阴极中加入硝酸盐(nitrate)时,可逆峰转变为S型,阴极电流显著增加。这些结果证实了电子穿梭体有效地增强了硝酸盐还原速率并降低了过电位。与NR和RF相比,POH介导的硝酸盐还原显示出更正的起始电位,并且还原电流高于NR。更重要的是,这一起始电位非常接近希瓦氏菌中硝酸盐还原酶的热力学限制。因此,POH被选为后续研究的最佳电子穿梭体。
B. 光阳极的性能:
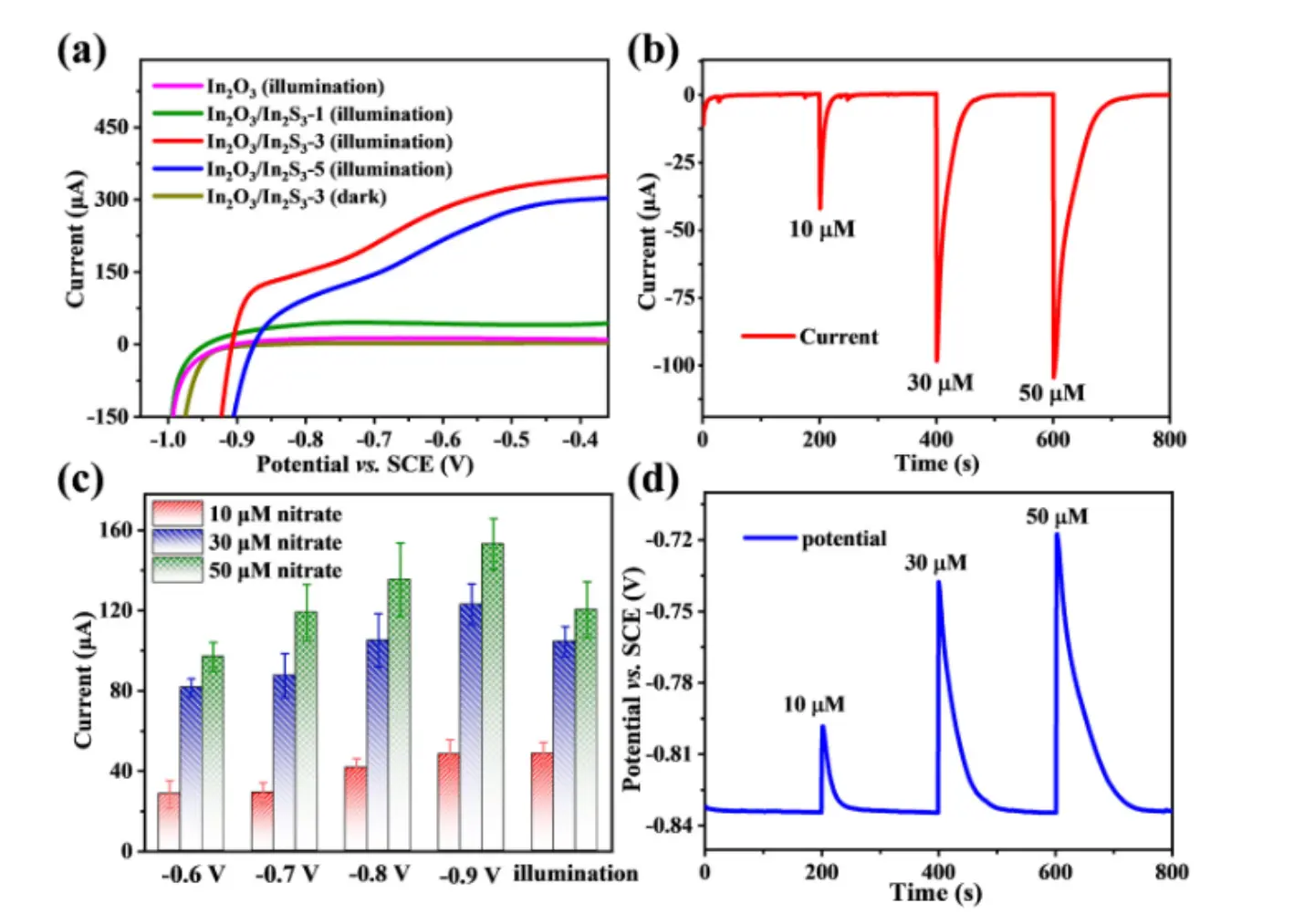
图 2 光驱动生物阴极传感器的光电化学特性及对硝酸盐的响应分析
通过UV–vis DRS测量光阳极的光吸收能力,发现In₂O₃/In₂S₃光阳极在可见光区域具有广泛吸收范围,最大吸收在500 nm以下。如图2a,LSV分析表明,In₂O₃/In₂S₃-3光阳极表现出较低的起始电位(-0.9 V)和较大的阳极电流(277 µA@-0.6 V),优于In₂O₃/In₂S₃-5。此外,In₂O₃/In₂S₃-3在无光照时仅产生背景电流,表明其光电化学特性显著,可为生物阴极提供动力。基于此,通过短路连接In₂O₃/In₂S₃-3光阳极和生物阴极,构建了双室光驱动生物阴极还原系统。如图2b,在有光照但无硝酸盐时,背景电流迅速衰减至<1 µA,表明副反应可忽略;加入10 µM硝酸盐后,电流响应迅速上升后逐渐衰减,表明反向电子传递成功建立且硝酸盐被消耗。进一步实验表明,加入更高浓度硝酸盐(30 µM和50 µM)时,电流响应趋势类似,但加入10 µM硝酸盐时的峰值电流更高。
如图2c,在三电极体系中,生物阴极对硝酸盐的安培响应趋势与光驱动生物阴极相似,但峰值电流略有差异。如图2d,研究者通过另一个电化学工作站同时测量了光驱动生物阴极还原过程中生物阴极的电极电位,发现生物阴极电位对硝酸盐添加表现出动态响应。无硝酸盐时稳定在约-0.84 V,加入硝酸盐后电位正向移动。这表明光阳极供电负担低,硝酸盐还原加速导致光阳极过电位增大,电极电位正向移动。因此,整个系统的动力学瓶颈在于光阳极,生物阴极在一定浓度范围内可高效还原硝酸盐,为定量分析奠定了基础。
C. 传感器的开发:
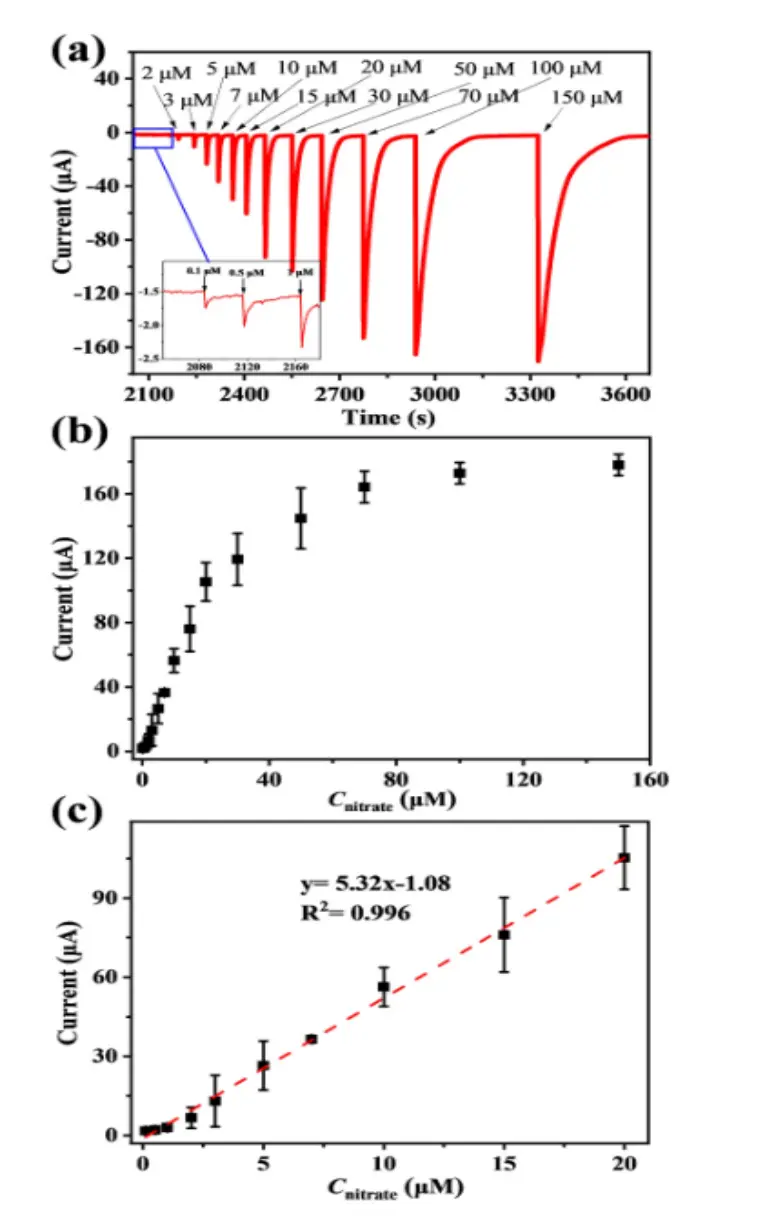
图 3 光驱动生物阴极传感器对硝酸盐剂量的电流响应
生物传感器由LED驱动的In₂O₃/In₂S₃-3光阳极、MR-1悬浮液生物阴极和碳布电极组成。在无硝酸盐时记录背景电流,稳定后注入硝酸盐水样并记录电流变化。如图3a,低至0.1 µM的硝酸盐即可引起即时电流响应,且单次检测仅需几十到几百秒,远快于传统生物阳极传感器(需近1小时)。
如图3b和3c所示,随着硝酸盐浓度增加,峰值电流在0.1–20 µM范围内呈线性关系,灵敏度为5.32 µA µM⁻¹,检测限为0.028 µM。当浓度超过50 µM时,峰值电流趋于饱和(150 µM时为178 µA),这可能是由于光阳极和生物阴极的动力学限制。与传统方法相比,该传感器具有更高的灵敏度和更低的检测限。
D. 生物传感器的检测性能
在应用于实际样品测试之前,本研究对所开发的生物传感器的选择性、可重复使用性、准确性和稳定性进行探究。
a) 选择性:研究发现在高浓度(1 mM)的常见阴离子(氯离子、硫酸根离子、碳酸根离子)存在下,电流响应变化小于1 µA,表明传感器对硝酸盐具有良好的选择性。即使在亚硝酸盐存在时,通过基因敲除亚硝酸盐还原酶(ΔnrfA),传感器对硝酸盐的选择性显著提高,响应电流主要反映硝酸盐的浓度。
b) 可重复使用性:连续10次测量10 µM硝酸盐水样时,电流响应略有衰减,可能是由于光阳极的部分光腐蚀。在4°C下储存光阳极30天,未观察到电流响应衰减,表明光阳极具有良好的储存稳定性。
c) 准确性和重复性:通过向水样中添加1–15 µM硝酸盐进行测试,回收率为91.5%–111%,变异系数(CV)为0.7%–8.8%,表明传感器具有高准确性和重复性。
3、实际应用
将生物传感器应用于生物反应器水样的检测,结果与传统比色法一致(偏差小于10%),表明该传感器具有良好的抗干扰能力和实际应用潜力。
4、创新点
1、开发了一种用于硝酸盐检测的光驱动全细胞生物阴极传感器。
2、In₂O₃/In₂S₃光阳极高效驱动生物阴极,并与其动力学特性相匹配。
3、生物阴极电位能够动态响应不同剂量的硝酸盐。
4、实现了0.1–20 μM的线性检测范围和0.028 μM的检测限。
原文链接:https://doi.org/10.1016/j.snb.2024.136761
文章来源:微生物安全与健康网,作者~梁冬雪。





