细胞慢病毒转染预实验方案分享
发布时间:2025-02-24 浏览次数:2453
1.预实验目的:确定慢病毒对细胞的感染MOI和最佳的感染条件,为正式实验提供参考,如感染试剂的选择,感染时的总体积感染后换液的时间等。
2.预实验分组:按照不同培养条件将实验分为4组。分别为:
Ⅰ、Control组(C组):监控实验过程中细胞生长是否正常(加入完全培养基,不含病毒和助转染试剂)
Ⅱ、接毒组(M组):观察常规培养条件下病毒对细胞的感染效果(首先用阴性对照(NC)病毒来摸条件,加入一定量的完全培养基和病毒液)
Ⅲ、病毒液+HiTransG A(助转染试剂)组(A组):观察HiTransG A是否可以提升感染效果(完全培养基+HiTransG A+NC病毒液)
Ⅳ、病毒液+HiTransG P(助转染试剂)组(P组):观察HiTransG P是否可以提升感染效果(完全培养基+HiTransG P+NC病毒液)
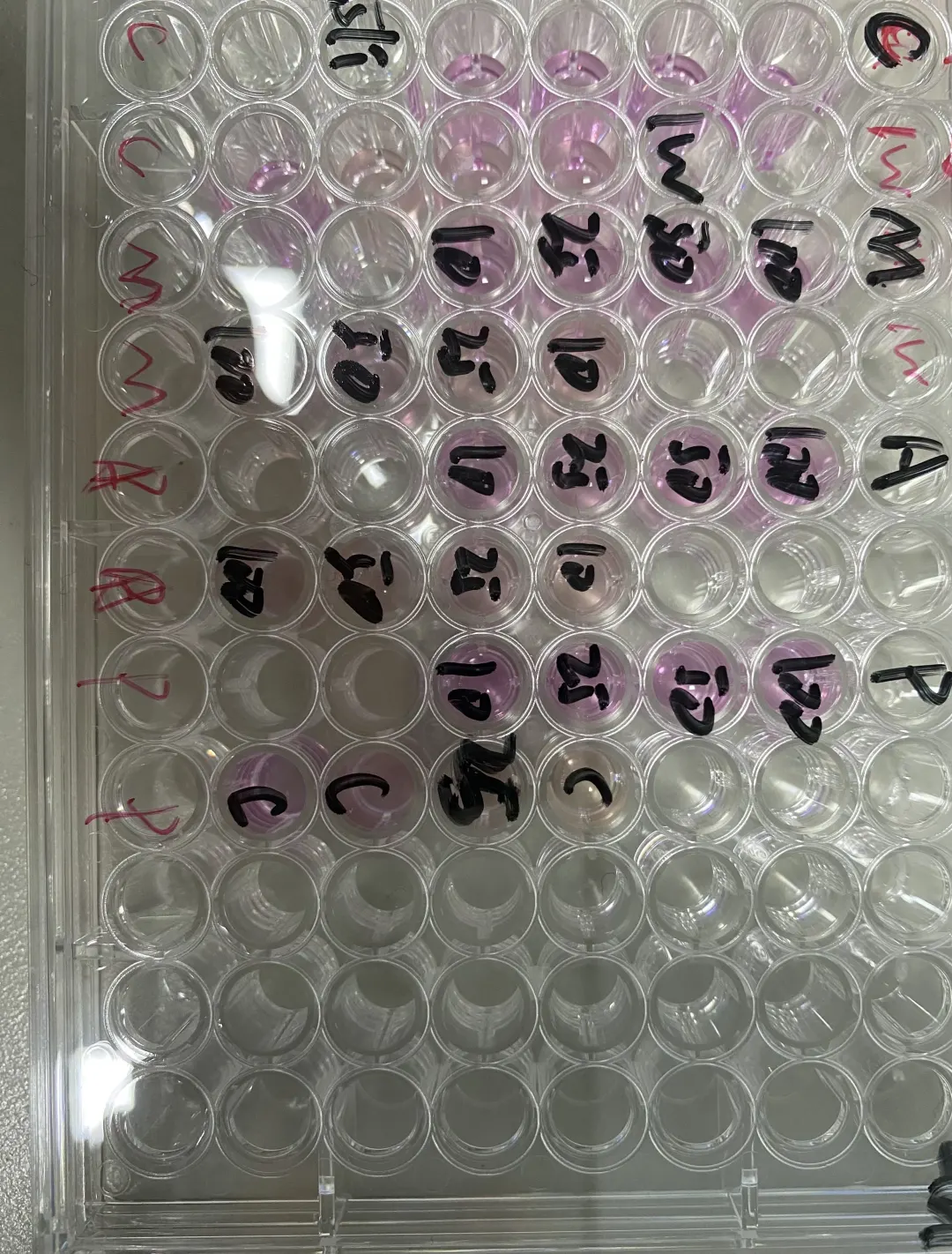
3.预实验操作方案
3.1.贴壁细胞
Day1:接种细胞:用完全培养基制备3ml密度为3~5×104个/ml细胞悬液。具体细胞密度可根据实验所用的细胞生长情况及大小进行调节,取100µl加入96孔板中,共16个孔,其中3个孔作为Control组,37°C 培养16-24h,至细胞汇合度为20-30%(也可直接铺板时时直接铺20-30%的细胞,,贴壁较快的细胞等待4-6h及可进行接毒)对于大部分细胞,我们通常认为培养24h后细胞数量是铺板时数量的两倍,每孔细胞数量约1W。
Day2:感染
Ⅰ、从冰箱取出病毒,冰上融化。用完全培养基依次将病毒稀释至滴度1x10^8 TU/ml, 5x10^7TU/ml, 2.5x10^7TU/ml, 1x10^7TU/ml,稀释完成后每组最少35µl。
Ⅱ、吸掉各孔中上清液,按照表1更换培养基, 加入病毒及相应感染增强液, 混匀,继续培养。感染后16-24h用完全培养基进行换液,过程中观察细胞形态,发生变化时可以提前到8h换液, 保持细胞正常生长。
表1.预实验分组及感染
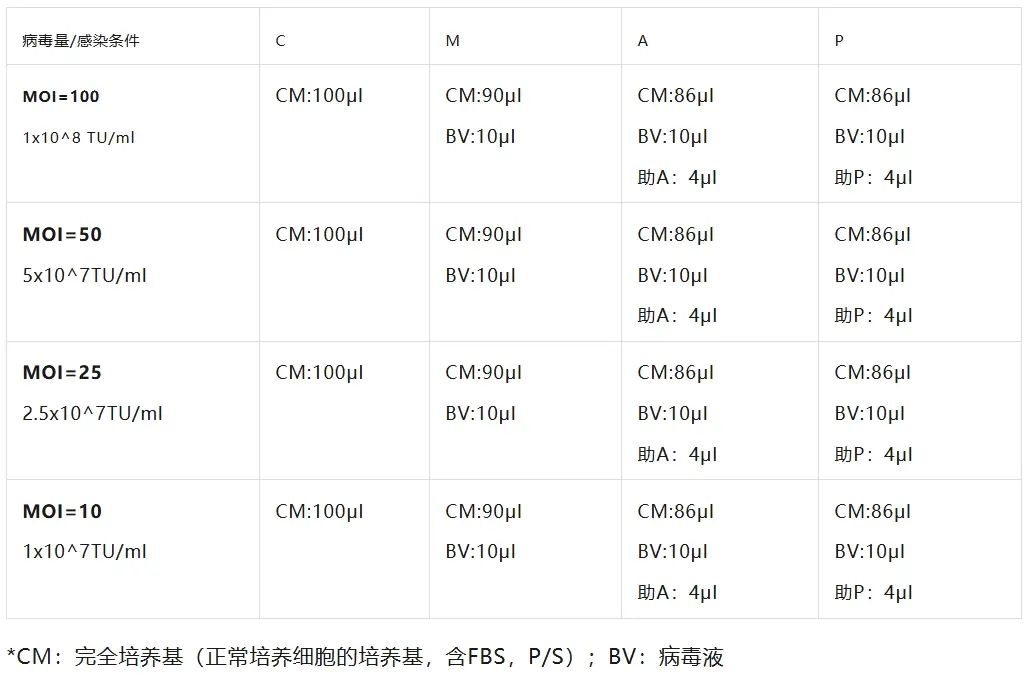
Day3-4:继续培养:中途可根据细胞的生长状况进行换液,保持细胞活性。
Day5:感染效果确认:感染约72-96h,荧光表达丰度较高时,用显微镜观察。感染效率80%左右,且细胞生长良好的组所对应的感染条件和MOI即可以作为后续感染实验的依据。
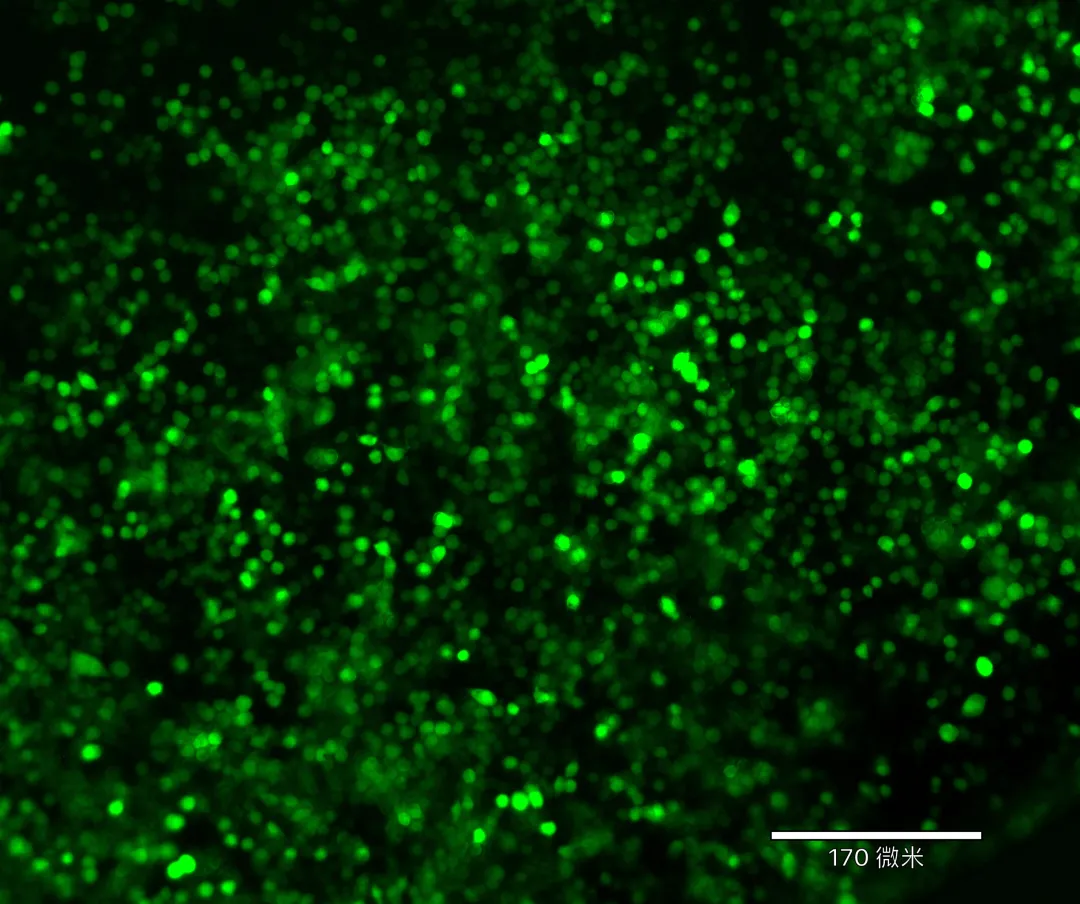
3.2.悬浮细胞
相对于贴壁细胞,悬浮细胞在第一天即可完成接种和感染操作,且接种细胞数量需在1W左右 cells/孔,接种时同时感染病毒,感染8-24h,根据细胞生长情况进行加液操作,无需换液,以免损失细胞。其余操作同贴壁细胞。
3.3.半悬半贴细胞
实验方案:略。建议参考悬浮细胞操作方案进行。
注解:
MOI: 复感染指数,是指病毒对细胞的感染能力,MOI越高,细胞越难被感染。通常把某株细胞有80%被感染时所用的病毒颗粒数和细胞数目的比值作为该株细胞的MOI。
MOI=(病毒滴度 × 病毒体积) / 细胞数目
HitransG A :吉凯基因自主研发的病毒感染增强液。它的主要成分是一种新型的高分子非离子表面活性剂,同时也是一种细胞保护剂和促进吸收剂。它可以通过提高细胞表面活性,增加病毒与细胞的接触面积,促进病毒高效感染细胞,且对细胞毒性极低,适合敏感细胞使用。
HitransG P:吉凯基因自主研发的病毒感染增强液。它的主要成分是一种阳离子聚合物,通过抑制细胞膜与病毒之间的电荷排斥, 增加慢病毒对细胞的感染效率。本产品可以极大提高细胞感染效率,且细胞毒性显著低于Polybrene。
参考资料:GE042.6重组慢病毒载体使用手册
文章来源:环凯转载于“ 爱吃洋芋的酸菜鱼”公众号;原标题:“细胞慢病毒转染预实验方案分享”;作者~ GAPDH。
转载声明:本文为转载发布,仅为分享学习目的。对转载有异议和删稿要求的原著方,可联络站点客服删除。






